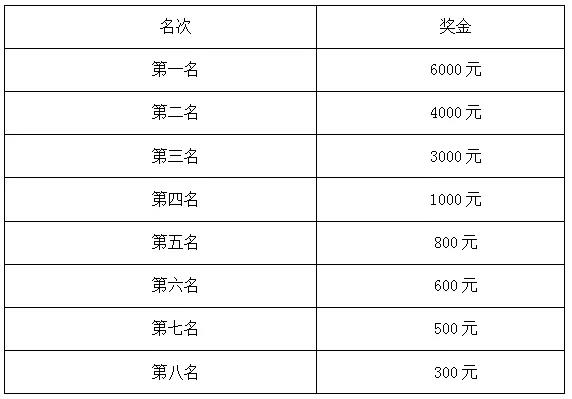
2023年6月22日,一种名为Elevidys的药物获得FDA加速批准。随后,这款售价320万美元(约合人民币2306万元)一个疗程的新药迅速登上榜单,成为全球第二贵的药物。然而,Elevdys的推出并没有引起预期的热烈欢迎。包括Nature在内的权威医学媒体和医学专家都对这款药物的前景持观望态度。研发药企股价不升反降。
《自然》报告将“内部反对”列为标题
世界第二贵的产品,它是如何诞生的?
Elevidys是生物制药公司Sarepta和罗氏联合开发的基因治疗药物,用于治疗杜氏肌营养不良症(DMD)患者。此次获批后,该药物也成为全球首个上市的DMD基因治疗药物。
DMD是一种罕见的遗传性肌肉疾病,婴儿发病率为1/3300[1],致残率极高。典型的 DMD 最早可在 2 至 3 岁时出现。到12~13岁时,患者只能依靠轮椅生活,平均寿命不足20岁[2]。
DMD 是由肌营养不良蛋白基因失活突变引起的。在肌肉中,肌营养不良蛋白具有保护肌纤维细胞膜、防止运动后肌肉疲劳、防止钙离子病理性流入肌纤维的功能。然而,DMD患者严重缺乏肌营养不良蛋白,导致肌纤维严重退化[3]。这反过来又导致肌肉组织的结构紊乱和功能丧失。
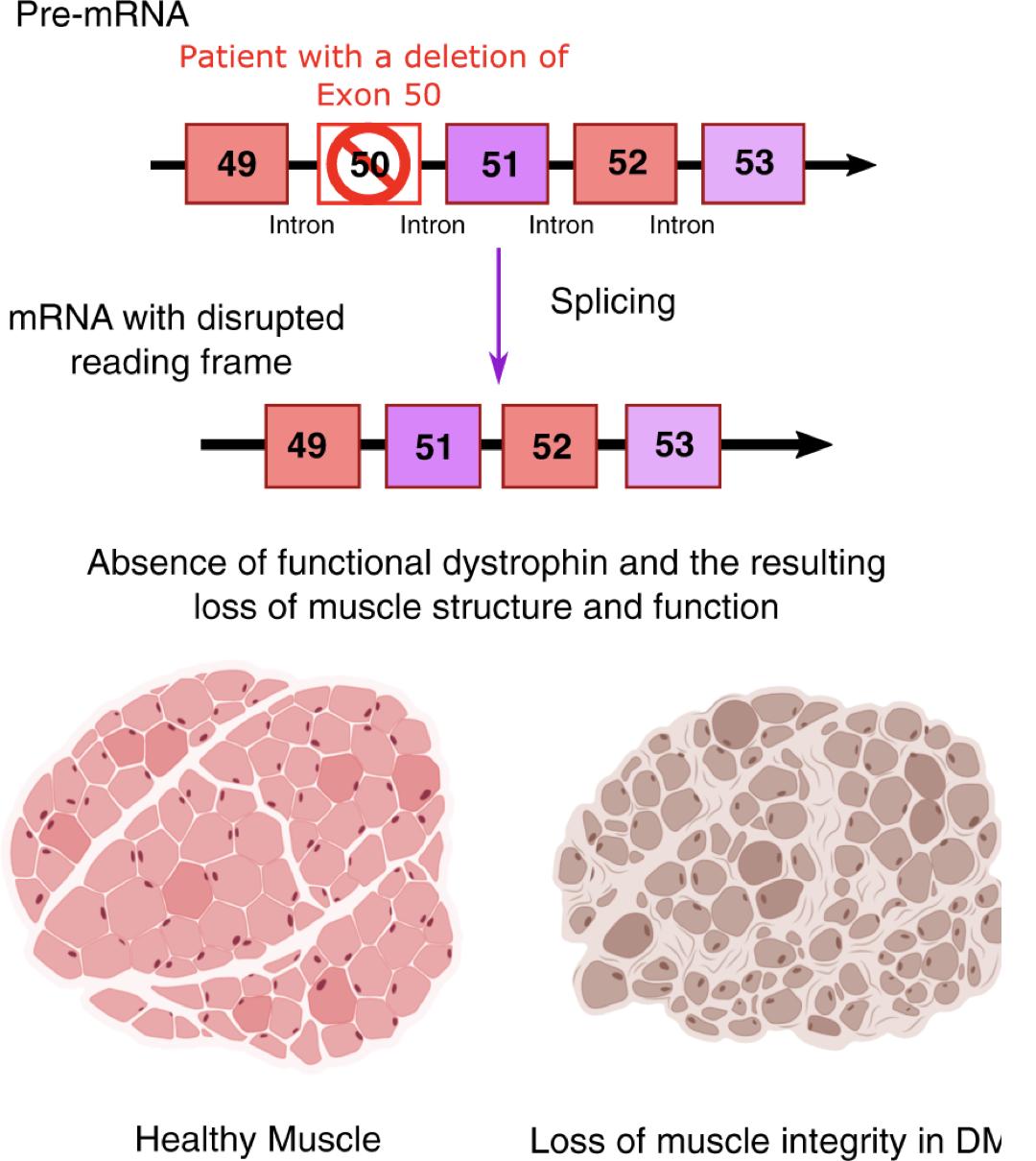
一种常见的肌营养不良蛋白基因突变(外显子50缺失)导致DMD患者的肌肉(图中右侧)结构紊乱,使肌纤维和其他支持细胞难以形成正常肌肉(来源:参考文献4)
这种病该如何治疗呢?
理论上,与其他遗传病类似,如果能够利用载体将正常的肌营养不良蛋白基因导入肌纤维中,让肌纤维分泌正常的肌营养不良蛋白,那么患者或许能够恢复正常的肌肉功能。不幸的是,这个看似天真无邪的想法在现实中遇到了瓶颈:肌营养不良蛋白基因是迄今为止最大的人类基因,而一些常用的基因治疗载体,如腺相关病毒(AAV),无法完成将基因带入体内的过程。它的基因组。
为了克服这个问题,研究人员试图从旧的经验中寻找新的解决方案。
早在20世纪80年代,就有学者发现,一些DMD患者虽然存在基因突变,不能产生完整的肌营养不良蛋白,但他们的身体仍然可以合成丢失了部分氨基酸片段的截短型肌营养不良蛋白。阿托品,这些蛋白质仍然可以在体内发挥作用,也正因为如此,这组患者的症状明显比普通患者轻[5]。

如果无法传输完整的基因,则传输截短的版本。这已成为DMD基因治疗研发的核心理念。最后,在选择了功能保存最好的截短抗肌营养不良蛋白后,研究人员将其基因插入到rh74腺相关病毒(一种源自非人类灵长类动物的腺相关病毒)载体中,万众期待的Elevidys诞生了。
加速审批后功效遭质疑
作为生物制药公司Sarepta的核心产品,Elevidys自宣布研发以来就引起了广泛关注。就连全球十大研发药企之一的罗氏公司,2019年也向Elevdys投资了11.5亿美元(约83亿元人民币,其中7.5亿美元现金和4亿美元股权),以支持其研发,并根据研发进度和销售情况,还为 Elevidys 设定了高达 17 亿美元的里程碑付款[6]。不仅如此,Elevdys的发展恰逢基因治疗的红利期。这种“极其昂贵但一次性治愈罕见疾病”的治疗方法正在被越来越多的患者接受。从基因治疗机制来看,一旦Elevidys获批,几乎所有DMD患者都有可能从中受益。
然而谁也没想到,Elevidys获批上市后,等待的并不是想象中的鲜花和掌声,而是来自现实的严厉打击——研发制药公司Sarepta的股价应声下跌11%。媒体和医学界的质疑随之而来。首先是Elevodys的功效。在FDA关于该药物上市的专家咨询委员会会议上,专家们以8-6分的微弱优势批准了该药物的加速上市,使该药物成为史上唯一在没有确凿证据的情况下通过加速审评程序上市的药物。功效。基因治疗药物[7]。

Elevidys 的 FDA 批准文件
在这一加速上市批准中,替代终点是在患者骨骼肌中观察到的截短肌营养不良蛋白的表达。许多评论家认为,这一终点仅意味着Elevidys已成功将该基因导入肌纤维并稳定表达。但目前尚无强有力的证据表明这种表达是否与患者临床症状的改善有关。在该药的II期临床试验中,治疗组患者在第12周时的肌肉活检显示,肌纤维肌营养不良蛋白水平已达到正常人的40%左右;然而,在第48周的步行能力评估量表中,治疗组和安慰剂组之间的得分没有差异。进一步分析表明,Elevidys 成功改善了 4 至 5 岁儿童的步行能力,但对 6 至 7 岁儿童没有效果[7]。正是因此,FDA在Elevdys的审批中增加了4至5岁的严格年龄限制[8],预期的全面批准改为加速批准。
一个疗程2300万,但不一定能赚钱
伴随着质疑和争议,研发药企公布了Elevidys的售价:每个疗程320万美元(约合人民币2306万元)。这个价格已经挤掉了每个疗程售价300万美元的Skysona(一种治疗肾上腺脑白质营养不良的基因治疗药物),成为全球第二贵的药物,仅次于去年批准上市、售价为美国的Hemgenix每个疗程 350 万美元。 (血友病 B 的基因治疗药物)。
不过,市场分析并不看好这样的高价能带来多少收入。一份报告预测,今年只有 9 名患者可能接受 Elevidys 治疗;另一项分析预测,今年将有 59 名患者使用 Elevidys,总销售额约为 1.17 亿美元(约合人民币 8.4 亿元)——这距离之前设定的 17 亿美元的销售里程碑还相去甚远。 Elevidys 的情况并非孤例。事实上,很多昂贵的药品并没有想象中那么有利可图。目前,在全球药品价格排行榜中,排名前5位的药物无一例外都是基因治疗药物。
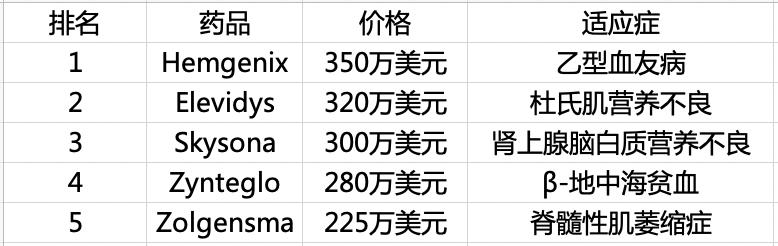
当前全球前5大药品价格(来源:自制,根据FiercePharma《2023年最贵药品报告》整理)

虽然基因疗法理论上可以一次性治愈一种疾病,但大多数时候它并不是不可替代的。
比如治疗B型血友病的Hemgenix,美国大部分商业医疗保险公司都宣布不报销该药的费用,或者只报销对市面上所有药物都无效且终生的患者。期待足够长。与保险全额承保的凝血因子替代治疗相比,尚未表现出压倒性的竞争力。
其次,对于大多数基因治疗药物来说,其能够覆盖的患者群体相对较小,能够真正使用该药物的患者群体就更少了。
比如刚刚批准的Elevidys,就从原来的适应症4~7年缩短到了4~5年。此外,FDA要求在使用该药物前筛选抗AAVrh74抗体。这导致适合该药物的患者数量急剧下降。减少到每年约 400 人。不仅如此,基因治疗仍然是一个风险与收益并存的领域。
以Elevidys使用的AAV为例,有研究[9]表明,健康人产生AAV6抗体的概率高达40%。如果对已有抗AAV抗体的患者进行基因治疗,将存在失去疗效甚至严重免疫不良反应的风险。风险[10][11]。此外,许多 AAV 本身对人类具有很强的免疫原性。去年10月,美国一名27岁的晚期DMD患者在临床试验中接受了以AAV为载体,利用CRISPR-Cas9基因编辑技术重新编辑肌营养不良蛋白基因的治疗。 8天后,他因脑损伤和多种并发症去世。死于器官衰竭。
尸检结果显示[12],研究人员错误估计了患者的残余肌肉体积,并过量服用了药物。大量的载体病毒在患者体内诱发毛细血管渗漏综合征,并迅速导致患者出现急性呼吸窘迫综合征,最终死亡。此前另一家公司以AAV9为载体的DMD基因治疗药物的临床研究中,患者接受载体病毒注射后,免疫系统产生针对载体病毒衣壳的免疫反应,进而攻击心肌细胞,导致何先生出现心源性休克,心力衰竭,最终死亡。结果,该药的研发被FDA暂停4个月。
上述因素影响了基因治疗药物的销售和推广。然而,基因治疗也并非没有例外。 Zolgensma,一种治疗脊髓性肌萎缩症的基因治疗药物,已成为诺华意想不到的利润焦点。
作为全球第四贵的药物,Zolgensma 一个疗程的售价为 225 万美元。该药上市后第一季度销售额达到1.6亿美元。 2021年销售额将高达13.51亿美元,2022年销售额将进一步升至13.7亿美元[14],甚至高于口服药物Listralan(2022年销售额为11.73亿美元),该药物也治疗脊椎肌肉萎缩症萎缩。 Zolgensma之所以如此受欢迎,一方面是因为脊髓性肌萎缩症是一种比较常见的罕见病,患者数量较多;另一方面,脊髓性肌萎缩症是一种比较常见的罕见病,患者数量较多。另一方面,Zolgensma治疗相对简单,不良反应也较少。回到新获批的Elevidys,虽然前景仍不明朗,但研发药企表示将继续开展III期临床试验,尽快扩大适应症范围。制药公司还表示,Elevidys的售价甚至可以达到500万美元至1300万美元。只有这个价格,药物才“划算”。
参考
[1]美国食品和药物管理局。 FDA 批准首个基因疗法用于治疗某些杜氏肌营养不良症患者。
[2] Passamano L、Taglia A、Palladino A 等人。杜氏肌营养不良症患者生存率的改善:835 名患者的回顾性分析。阿克塔·迈奥尔。 2012;31(2):121-5。
[3]Ervasti JM、Ohlendieck K、Kahl SD 等人。营养不良的肌肉中肌营养不良蛋白复合物的糖蛋白成分缺乏。自然。 1990;345(6273):315-9。号码:10.1038/345315a0

[4]希米奇 V,戴维斯 KE。评估新型遗传方法治疗杜氏肌营养不良症的潜力。欧洲流行基因杂志。 2021;29(9):1369-1376。 DOI:10.1038/s41431-021-00811-2
[5]摩纳哥 AP、Bertelson CJ、Liechti-Gallati S 等人。对 DMD 基因座部分缺失的患者之间表型差异的解释。基因组学。 1988;2(1):90-5。内线:10.1016/0888-7543(88)90113-9
[6] F. Hoffmann-La Roche Ltd. 罗氏与 Sarepta Therapeutics 签订许可协议,以改善杜氏肌营养不良症患者的生活。
[7]Mullard A. 尽管内部存在反对意见,FDA还是批准了首个针对杜氏肌营养不良症的基因疗法。 Nat Rev 药物发现。 2023 年 6 月 23 日。doi:10.1038/d41573-023-00103-y
[8]由于对 Elevidys 标签扩张潜力的担忧,BioSpace.Sarepta 股价下跌。
[9]曹琳,莱德波尔A,潘Y,等。临床入组检测,用于检测预先存在的 AAV6 中和抗体,并在基因治疗试验中证明转基因表达。吉恩·瑟尔. 2023;30(1-2):150-159。 DOI:10.1038/s41434-022-00353-2
[10]Bucher K、Rodríguez-Bocanegra E、Dauletbekov D 等。使用腺相关病毒载体对视网膜基因治疗的免疫反应 - 对治疗成功和安全的影响。视网膜眼科研究进展。 2021;83:100915。 doi:10.1016/j.preteyeres.2020.100915
[11]West C、Federspiel JD、Rogers K 等人。腺相关病毒中和抗体复合物激活补体。嗯,吉恩·瑟尔。 2023;34(11-12):554-566。 doi:10.1089/哼。 2023.018
[12]Lek A、Wong B、Keeler A 等。在 rAAV9 递送的 CRISPR 反式激活剂的 N-of-1 试验中,一名杜氏肌营养不良症患者意外死亡。 medRxiv 2023.05.16.23289881。 doi:10.1101/2023.05。 16.23289881
[13]Lek A、Atas E、Hesterlee SE 等。会议报告:2022 年肌营养不良协会峰会“基因转移治疗的安全性和挑战”。神经肌肉疾病杂志。 2023;10(3):327–36。
[14]诺华公司。产品销售:2022 年全年产品销售。
本文来自微信公众号,作者:邓橙,36氪经授权发布。
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请联系本站,一经查实,本站将立刻删除。如若转载,请注明出处:https://www.xcdzgl.com/html/tiyuwenda/6042.html